Учебные материалы
Конектбиофарм
Работа
Компании
Реклама от Google
Костные клетки
Родоначальные клетки костной и хрящевой тканей
Костные клетки имеют мезенхимальное (мезенхимное, мезодермальное) происхождение. Во взрослом организме они образуются из остеогенных стволовых клеток-предшественников, которые локализуются на границе между костью и хрящевой или костномозговой тканью. Дифференцируясь, они превращаются в остеобласты, а затем - остеоциты. Рост длинных трубчатых костей осуществляется путем энхондрального окостенения. Причем увеличение диафизов в ширину происходит только со стороны периоста, а метафизов - только со стороны эндооста. Процесс костной резорбции имеет, соответственно, обратное направление (Burne, 1971, 1976; Фриденштейн, Лалыкина, 1973).
Схема образования костной и хрящевой ткани, построенная на основании работ А.Я. Фриденштейна, Е.А. Лурия (1980), А.Я. Фриденштейна и др. (1999), И.Л. Черткова, О.А. Гуревич (1984), В.П. Шахова (1996). Н. Castro-Malaspina et al., (1980, 1982) с некоторыми модификациями, представлена на рисунке.
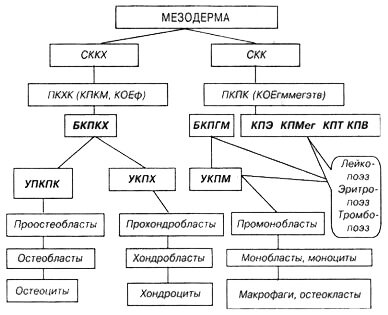
Схема остеогенеза, хондрогенеза и остеокластогенеза. СККХ - стволовая клетка костной и хрящевой ткани, СКК - стволовая клетка кроветворения, ПКПК - полипотентная клетка-предшественница кроветворной ткани, ПКХК - полипотентная клетка-предшественница для костной и хрящевой тканей, Б(У)КПКХ - би(уни)потентная клетка-предшественница костной и хрящевой ткани, КПКМ - клетка, переносящая кроветворное микроокружение, КОЕф - колониеобразующая единица фибробластов, У (Б) КПК (X, М, Г, Э, Мег, Т, В) - унипотентная (бипотентная) клетка-предшественница костной (хрящевой, макрфагальной, гранулоцитарной, эритроидной, мегакариоцитарной, Т и В-лимфоидной) ткани
Процесс образования костной ткани представляет собой сложный многоступенчатый процесс, при котором клетки различных гистогенетических линий проходят последовательную трансформацию путем пролиферации, дифференцировки и специализации с образованием композитной структуры, называемой костью.
При этом следует подчеркнуть, что если костная и хрящевая ткань формируется в эмбриогенезе из дорсального сомита мезодермы, то кроветворная ткань, из которой ведут свое происхождение остеокласты, - через стадию спланхнической мезодермы. По своему гистогенезу остеоциты и остеобласты ближе к соединительно-тканным, мышечным и кожным элементам, а остеокласты - к клеткам крови и эндотелию (Coalson, 1987). Наличие в остеокластобластомах эпителиальной и мышечной ткани, по-видимому, подтверждает эту точку зрения.
После расхождения направления развития остеохондрогенеза от гемопоэза в эмбриональном развитии, в зрелом организме процесс образования костных клеток осуществляется из более дифференцированного, фиксированного в тканях или циркулирующего незрелого стромального элемента (мезодермальной клетки, недифференцированного фибробласта, остеогенного предшественника или прекурсора) (Фриденштейн, Лурия, 1980; Альберст и др., 1994; Омельянченко и др., 1997). Наряду с наличием полипотентной стволовой клетки для костной и хрящевой ткани, существуют и более дифференцированные прекурсоры. СККХ имеют высокий пролиферативный потенциал, обладают полипотентностью. Они образуют, как минимум, костные и (или) хрящевые кариоциты, которые преимущественно находятся в G1-G2-стадии клеточного цикла (Фриденштейн, Лалыкина, 1977; Фриденштейн, Лурия, 1980; Фриденштейн и др., 1999; Чертков, Гуревич, 1984).
В культуре ткани in vivo и in vitro они образуют хрящевую или костную ткань, которая может быть представлена в форме колоний, обозначенных как колониеобразующие единицы фибробластов-КОЕф (Фриденштейн, Лурия, 1980). С помощью хромосомных и биохимических маркеров на радиационных химерах было показано, что КОЕф имеют клональную природу, отличную по своему происхождению от гемопоэтических клеток костного мозга, включая остеобласты и остеоциты (Чертков, Гуревич, 1984).
Нами в суспензионной культуре ткани костного мозга мышей линии Balb/c была изучена зависимость между количеством вводимых в среду кариоцитов и числом образовавшихся колоний. Для этого костный мозг вымывался в силиконизированную пробирку, суспендировался в D-MEM среде, содержащей 20% эмбриональной телячьей сыворотки, 40 мкг/мл гентамицина, 200 мМ, L-глютамина хепес и культивировался в течение 2-3 недель в пластиковых флаконах при 37 °С. Плотность посева составила от 104 до 107 клеток на мл.
Зависимость образования КОЕф при введении в культуру различного количества клеток костного мозга мышей линии Balb/c
| Количество вводимых клеток | Число образовавшихся колоний |
| 104 | 0 |
| 105 | 12 |
| 106 | 27 |
| 107 | 31 |
Приведенные данные свидетельствуют о том, что в целом зависимость между количеством вводимых в культуру миелокариоцитов и КОЕф носит линейный характер, что еще раз подтверждает их клональное происхождение.
При трансплантации их под капсулу почки или под кожу, они обладают способностью формировать костную, либо хрящевую ткань.
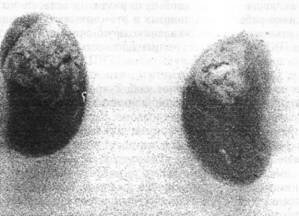
Макроскопический препарат эктопической костной ткани, выросшей под капсулой почки после трансплантации в нее костного мозга стрессированных мышей F1(CBAxC57Bl). Слева - на верхнем полюсе органа отчетливо виден большой очаг костеобразования. Справа - контроль (костный мозг взят от нестрессированного животного)
Одним из свойств СККХ является то, что они сохраняют свои пролиферативные и дифференцировочные потенции при многократном переносе первоначальной культуры от одного донора к другому. По-видимому, повреждение генома на этом уровне приводит к образованию остеосарком.
В результате дифференцировки СККХ образуются более дифференцированные клетки-предшественники типа КПКХ (клетки предшественники для костной и хрящевой ткани) или БКПКХ (бипотентные), затем - УПКПК и УПКПХ (унипотентные для кости, либо хряща). Общей закономерностью для пула родоначальных клеток любой ткани, в том числе и костной, является постепенное снижение способности к самообновлению и пролиферации, утрате полипотентности, увеличению доли прекурсоров, находящихся в S-периоде клеточного цикла, повышению чувствительности к действию ростовых факторов, гормонов, цитокинов и других регуляторных молекул. Теоретически этот процесс может идти равномерно или скачкообразно. Из-за этого течение остеогенеза может идти в различных режимах, темпе, с образованием костной ткани качественно и количественно отличной по своим морфофункциональным свойствам. На наш взгляд, введение биоматериала в кость обязательно включит тот или иной путь развития остеогенных клеток. Однако работ, выполненных в этом чрезвычайно интересном направлении, мы, к сожалению, не обнаружили.
Если ПКПКХ обладают полипотентностью, то БКПКХ образуют хрящевую или костную ткань, УКПК - только кость, а УКПХ - хрящ. Следует отметить, что все категории родоначальных клеток представляют собой чрезвычайно гетерогенную популяцию, внутри которой морфофункциональные свойства варьируют в широком диапазоне. Кроме того, для каждой из стадий развития КП имеется значительное количество переходных форм, которые все еще не могут быть идентифицированы с помощью имеющихся технологий. Несмотря на то, что методы выявления стромальных и остеогенных клеток-предшественников были открыты еще в начале 70-х годов, явного прогресса в понимании их свойств, способов регуляции и роли в процессах ремоделирования костной ткани достигнуто не было (Фриденштейн, Лалыкина, 1973; Фриденштейн и др., 1999; Чертков, Гуревич, 1984; Стецулла, Девятов, 1987; Омельянченко и др., 1997).
Следует отметить, что стволовые и коммитированные клетки-предшественники костной и хрящевой тканей находятся под контролем локальных и дистантных регуляторных механизмов. В последнюю группу входят факторы, которые оказывают свое действие через нейроэндокринную, иммунную, ретикулоэндотелиальную, опиатную, NO и другие системы путем выработки или связывания дальноранговых мессенжеров (эстрогены, глюкокортикоиды, эндорфины, адреналин и т.п.). Локальные механизмы действуют через прямое изменение морфофункциональных свойств микроокружения костной ткани, межклеточные контакты, местную выработку цитокинов, медиаторов, коротко-живущих биоактивных веществ и т.п. Межклеточные взаимодействия относятся к морфогенетическим процессам, они контролируют дифференцировку, специализацию, морфообразование клеток в тканях и органах. Механизмы их реализации осуществляются с помощью позиционно-информационных и индукционных взаимодействиях. Они еще малоизученны. Тем не менее, согласно концепции о позиционной информации, в организме существует морфогенетическое поле. Оно контролируется с помощью экспрессии гомейозисных генов типа НOХ1, НOХ2, НОХЗ, НOХ4, НOХ7, заставляя клетки помнить не только место своей локализации, в соответствии с координатными осями, но и выполнять миссию, которую они должны осуществить в процессе своей жизни, например восстановление кости при ее повреждении. Считается, что в сохранении позиционной информации большую роль играют мезенхимальные элементы, в частности макрофаги, остеобласты, остеоциты, остеокласты, эндотелий и фибробласты (Gilbert, 1994).
Индукционные механизмы регулируют процессы пролиферации и дифференцировки самообновляющихся клеточных популяций с помощью цитокинов, ростовых факторов, различных метаболитов и короткоранговых мессенжеров, вплоть до прямых клеточных взаимодействий.
Особенностью выбора направления дифференцировки поли- и бипотентных остеогенных предшественников является то, что он в первую очередь зависит от парциального давления кислорода. Если это давление достаточно высоко, то костные прекурсоры развиваются в направлении остеогенеза, а если низкое, то напротив, образуют хрящевую ткань (Bassett, Herman, 1961). При этом следует помнить, что адекватное поступление кислорода к клеткам возможно только при наличии развитой сети микроциркуляторного русла: максимальная величина удаления костных прекурсоров не должна превышать 100 мкм (Хэм, Кормак, 1983).
Система остеонов
Гаверсова система во взрослой кости постоянно обновляется. При этом всегда можно выделить несколько типов остеонов - эволюционирующих или развивающихся (5-10%), зрелых (50-75%), дегенерирующих или инволюционирующихся (10-20%), реконструирующихся (5-10%) и нежизнеспособных (5-10%).
Считается, что остеон (Гаверсова система) возникает только на основе туннеля, образующегося в результате действия моноцитов, макрофагов и остеокластов, заполняющегося изнутри концентрированными слоями костной ткани, формирующейся остеобластами и остеокластами (Хэм, Кормак, 1983). Следует отметить, что система остеонов представляет собой подвижную структуру, которая постоянно эволюционирует. Как это не парадоксально, работ, посвященных изучению кинетики остеонов, крайне мало. С помощью радионуклидных методов исследования было установлено, что годичная скорость замещения поверхностного слоя костной ткани составляет 5-10% (Harris, Heaney, 1969). По-видимому, и темп обновления остеонов имеет сходные параметры. Интересно, что диаметр остеонов в процессе развития не является постоянной величиной, а в течение всей своей жизни подвержен ряду последовательных изменений. Анализ литературных и собственных данных позволяет считать, что границы Гаверсовой системы, ограниченные линией цементации, у молодых, развивающихся и реконструирующихся остеонов составляют 80-150 мкм, зрелых - 120-300, а инволюцинирующих, дегенерирующих - менее 200 мкм. Если процесс образования остеонов протекает на границе надкостница/ кость, то вместо канала в начале формируется желобок, стенки которого выстланы остеогенными клетками, которые пролиферируют, формируя валик. Стенки этих клеточных выступов смыкаются, образуя полость, внутри которой, как правило, располагается не менее одной питающей артерии. Затем остеогенные клетки дифференцируются в остеобласты и остеоциты с формированием остеона. Предположения о том, что материал, используемый в травматологии, должен иметь диаметр пор равный размеру остеонов, высказывалось и ранее (Гюнтер и др., 1992). Однако этими авторами не был обоснован главный критерий, согласно которому размер пор должен соответствовать диаметру развивающихся, реконструирующихся, зрелых остеонов. При нарушении этого принципа в сторону увеличения или уменьшения диаметра пор полноценная костная ткань образовываться не будет. Иными словами, можно считать, что размер остеонов представляет собой важный морфообразующий фактор, который необходимо учитывать при создании искусственной костной ткани. Механизм этого феномена не совсем понятен. Он, вероятно, генетически запрограммирован в самих остеогенных клетках и является важным элементом костного микроокружения. Вместе с тем, следует подчеркнуть, что наряду с объемными характеристиками, например диаметром остеонов, при создании материалов необходимо учитывать и другие биологические принципы, речь о которых пойдет ниже.
А.В. Карпов, В.П. Шахов
Системы внешней фиксации и регуляторные механизмы оптимальной биомеханики